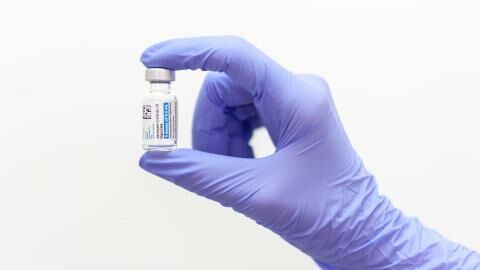
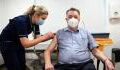
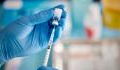
Wegen des Verdachts auf schwere Nebenwirkungen wie seltene Blutgerinnsel im Gehirn, an der wenige Menschen gestorben sind, hatten einige Länder in Europa die Verabreichung des Impfstoffes vorübergehend ausgesetzt, so auch Deutschland.
Nachdem die Impfungen nach der erneuten Prüfung vonseiten der Europäische Arzneimittelbehörde (EMA) wieder aufgenommen worden sind, werden nun die nächsten Zweifel laut.
AstraZeneca übermittelt Studie an USA
Obwohl der Impfstoff von AstraZeneca günstiger, leichter zu lagern und zu transportieren ist, als konkurrierende Impfprodukte, ist er in den USA noch nicht zugelassen.
Um diesen Prozess voranzutreiben, legt der Pharmakonzern eine Studie vor. Laut dieser war der Impfstoff zu 79 Prozent wirksam, um symptomatische Fälle von Covid-19 zu verhindern.
Die geimpften Probanden haben keine schweren Erkrankungen oder Krankenhausaufenthalte aufgewiesen. Bei Teilnehmern, die ein Placebo erhielten, traten fünf solcher Fälle auf.
Diese positiven Ergebnisse ähneln Berichten aus anderen Ländern. So fand man laut AstraZeneca auch bei unabhängigen Kontrollen kein erhöhtes Risiko für die gefürchteten Blutgerinnsel.
Doch für eine solche Schlussfolgerung ist die Studie zu klein. Insgesamt haben 30.000 Menschen in den USA, Peru und Chile daran teilgenommen. Nicht nur deswegen kommen nun erneute Zweifel auf.
Das Vertrauen in AstraZeneca schwankt
Die Ergebnisse der Studie sind noch in keiner Fachzeitschrift veröffentlicht oder von unabhängigen Forscherinnen und Forschern begutachtet worden, was die Glaubwürdigkeit deutlich unterstützen würde.
Das unabhängige amerikanische Data Safety Monitoring Board (DSMB), hält es außerdem für möglich, dass AstraZeneca mit veralteten Daten arbeitet, wodurch ein unvollständiges Bild der Wirksamkeitsdaten entstehen würde.
Das DSMB hat seine Bedenken gegenüber AstraZeneca kommuniziert, da bereits in den letzten Tagen Verzögerungen bei der Datenübermittlung aufgetreten sind. Eine Stellungnahme habe das Unternehmen bisher nicht abgegeben.
Ist da noch was zu retten?
In Kürze soll die geforderte Veröffentlichung in einem Fachjournal erscheinen und das U.S. National Institute of Allergy and Infectious Diseases (NIAID) stellt eine Forderung an AstraZeneca:
Wir fordern das Unternehmen auf, mit dem DSMB zusammenzuarbeiten, um die Wirksamkeitsdaten zu überprüfen und sicherzustellen, dass die genauesten und aktuellsten Daten so schnell wie möglich veröffentlicht werden.
Es wird sich also zeigen, wie verantwortungsbewusst der Konzern mit diesen Vermutungen umgeht und welche Ergebnisse in der nahen Zukunft im Bezug auf die Sicherheit von AstraZeneca vorliegen werden.